التفاعل الكيميائي مفهومه وقوانينه السنة الثانية اعدادي
مرحبا بكم أعزاءي في موقع JAMI3DOROSMAROC ، نقدم لكم شرح تفصيلي لدرس التفاعل الكيميائي مفهومه وقوانينه الثانية اعدادي، سنتعرف من خلاله على مفهوم التفاعل الكيميائي و قوانينه و كيفية تمثيله بالتجارب و الأمثلة.
 |
| التفاعل الكيميائي مفهومه وقوانينه السنة الثانية اعدادي |
مفهوم التفاعل الكيميائي
التفاعل الكيميائي هو تحول تختفي فيه مواد وتظهر فيه مواد جديدة ، كالاحتراقات على سبيل المثال تعتبر تفاعلات كيميائية.
- أثناء التفاعل الكيميائي يعاد توزيع الذرات المكونة لجزيئات المتفاعلات لتكوين نواتج تتكون ن جزيئات جديدة، مثال.
- C + O2 → CO2 (كما تلاحظ أن الناتج يحتوي على نفس نوع الذرات لكن بتوزيع مختلف عن المتفاعلات).
- يطلق على الأجسام المتفاعلة فيما بينها (كربون + ثنائي الأكسجين) اسم المتفاعلات و الأجسام الظاهرة (ثنائي أكسيد الكربون) بالنواتج.
مفهوم التحول الفيزيائي
التحول الفيزيائي هو تحول مادة معينة من حالة فيزيائية إلى حالة أخرى ، دون أي تعديل في طبيعة الجزيئات الخاصة بها ، كتحول كتحول الماء من الحالة الصلبة (الجليد) إلى الحالة السائلة.
كيفية تمثيل التفاعل الكيميائي؟
يمكن تمثيل تفاعل كيميائي معين :
- بالحصيلة ، مثال: ثنائي أكسيد الكربون → ثنائي الأكسجين + كربون.
- بالمعادلة الحصيلة (المعادلة الكيميائية)، مثال : C + O2 → CO2.
تذكير!
- علامة + قبل السهم تعني يتفاعل مع ، مثال ان كتبنا CH4 + O2 → CO2 + 2H2O ، فهذا يعني أن CH4 تتفاعل مع O2.
- علامة + بعد السهم تعني (و)، مثال ان كتبنا CH4 + O2 → CO2 + 2H2O ، أي أن هذا التفاعل الكميائي ينتج عنه CO2 و 2H2O.
نمذجة التحول الكيميائي
لمحاكاة التحول الكيميائي أو التفاعل الكيميائي شكليا، نستخدم النماذج الجزيئية أو الذرية للمتفاعلات والنواتج ، مع اشارتي (+ و →).
نمذجة التحول الفيزيائي
لمحاكاة التحول الفيزيائي شكليا، نستخدم النماذج الجزيئية أو الذرية للمتفاعلات والنواتج ، واشارة السهم فقط (→) ، لا نستعمل اشارة + لان التحول الفيزيائي لا يعد تفاعلا كيميائيا.
قوانين التفاعل الكيميائي للسنة الثانية اعدادي
 |
| قوانين التفاعل الكيميائي للسنة الثانية اعدادي |
قانون انحفاظ الكتلة
كتلة المتفاعلات تساوي كتلة النواتج.
الاختبار 1
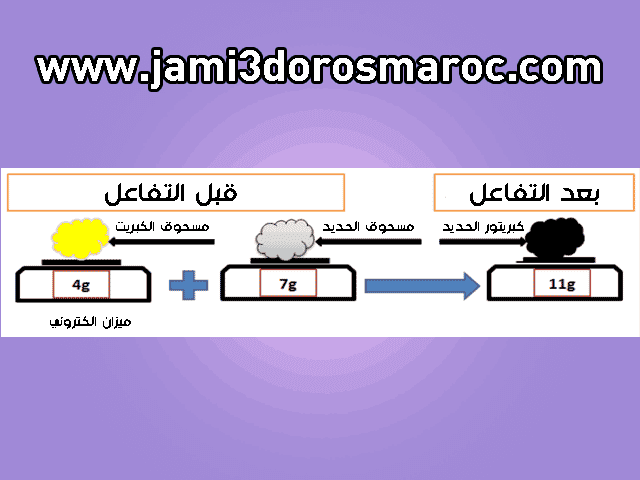
- نجلب 4g من مسحوق الكبريت و 7g من مسحوق الحديد.
- نمزجهما جيما ،ثم نسخن المزيج حتى التوهج باستخدام الموقد.
- ثم نزن كتلة النواتج بعد التفاعل.
 |
| قانون انحفاظ الكتلة |
ملاحظة
- نلاحظ تكون مادة سوداء تسمى بكبريتور الحديد.
- نلاحظ أن وزن النواتج يساوي وزن المتفاعلات، في هذه الحالة نقول أن الكتلة انحفظت.
قانون انحفاظ الذرات
عدد و نوع ذرات المتفاعلات يطابق عدد و نوع ذرات النواتج.
مثال:
عند احتراق الكربون C في ثنائي الأكسجين O2، ينتج جسم جديد يتكون من نفس عدد و نوع ذرات الأجسام المتفاعلة وهو ثنائي أكسيد الكربون CO2،في هذه الحالة نقول أن الذرات انحفظت.
 |
| قانون انحفاظ الذرات |

